一、定量核磁方法学研究案例分享
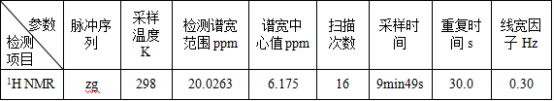
1.β-丙内酯定量核磁研究
1-1 项目名称
β-丙内酯定量核磁方法学研究
1-2 项目难点
β-丙内酯为无色有刺激气味的粘稠液体,易挥发,给样品称量增加了困难;
在加入内标(马来酸)的条件下,β-丙内酯中两个亚甲基的积分受弛豫延迟时间的影响较大,给其准确定量增加了困难。
1-3 解决途径及效果
样品称量过程时,将样品直接称量到液相小瓶中,称量完成后,直接加入相应的氘代试剂,并用封口膜密封,避免样品的挥发,解决了样品称量的问题;
通过调节弛豫延迟时间,让β-丙内酯中两个亚甲基的积分数值稳定,取数值稳定时较小的弛豫延迟时间进行检测,解决了样品积分不稳定的问题。
关键参数如下:
2.定量核磁研究服务与结构确证服务
我院服务优势
配备先进的仪器设备:百万分之一天平和600M核磁共振波谱仪,可以对化合物进行准确的称量和定量核磁分析检测;
项目经验丰富:结构确证团队项目经验丰富,研究项目涵盖天然产物、小分子化合物、多糖等大分子化合物的定量核磁分析研究,可提供分离、纯化、制备、结构确证、定量核磁的一条龙技术服务。
二、定量核磁干货分享
1.引言
本文总结了采集和处理定量1H、19F、31P和13C NMR数据的程序。需要注意的是,定量NMR(现在通常称为qNMR)不仅仅是收集一维光谱和比较积分的问题。为了获得准确和精确的定量结果,必须优化许多参数。定量NMR基本上有两种类型:
相对浓度测定
对于相对浓度测定,您需要将感兴趣的积分彼此进行比较。这将使您能够测量不同物种的准确比率,如果不是实际浓度本身的话。
绝对浓度测定
对于绝对浓度测定,您需要将目标积分与已知浓度标准品进行比较,并从这些绝对值得出浓度、产量和纯度。浓度标准品称为内标物或校准品,以区别于参比化合物,参比化合物可用于化学位移参考。
2.相对浓度测定
相对浓度测定是有机化学中最常见的定量NMR实验类型,也是最容易设置的。这种方法将为您提供混合物中化合物的比例。典型应用包括纯度评估和异构体比率测定。在制备样品时,请确保您的化合物可溶于所选溶剂,浓度足够高以产生良好的S/N,并且样品体积适合NMR。无需校准液。
3.绝对浓度测定
对于绝对浓度测定,除了上述有关样品制备的要点外,您的样品还应包含已知量的内标物。应尽可能准确地称量所有化合物。校准液不需要在结构上与目标分析物相关,但它确实需要包含目标原子核,并且具有不与分析物重叠的共振。如果校准剂产生相对简单的NMR波谱,只有单线态共振,这也是有益的。内标物的其他要求是它们应具有化学惰性、高度溶于所用溶剂、挥发性低且T1弛豫时间不是过长。
内标物的选择原则如下:
化学反应惰性
所选内标物不得与待测样品和所选的氘代溶剂发生反应。
溶解性
所选内标物应在所选的代溶剂溶解性好,至少要保证所称量的内标物在所用体积内的氘代溶剂中完全溶解,如果内标物没有完全溶解,则会造成目标化合物含量高于真实值。
分离度
所选内标物的特征峰应与待测样品的共振峰相分离,分离度不够容易造成积分不准确,从而影响化合物含量的结果准确性。内标物选择分离度提高存在困难时,可以尝试更换溶剂或者改用频率更高的仪器,以改善分离度。
内标物的溯源性
一般建议使用有证的可溯源性内标物,当获取有证的可湖源性内标物存在困难时,应能保证目前所用的内标物可溯源到有证的可溯源的标准物质。中检院常用定量核磁内标物:

如果校准液以纯形式存在且易于称量,这也是有益的。已经提出了几种常见的1H定量NMR内标物,表1中提供了一些更流行的示例:
表1 常见内标物性质及溶解性
4.定量需要考虑的信号
定量核磁共振当分析具有多个峰的波谱时,应明确分配用于定量的信号。此外,信号应尽可能简单,即单重态优于多重态,并且与其他峰的重叠尽可能少。活泼氢质子(如酰胺或羟基)不应用于定量,因为它们的范围很广并且对样品条件敏感。如果信号重叠是一个问题,可以通过改变溶剂或pH值或使用辅助Shift试剂来解决这个问题。
5.采集
5-1 参数设置
光谱仪上提供用于定量实验的特定参数设置。
默认情况下,1H和19F实验不使用13C去耦。这意味着,在对峰进行积分时(见下文),需要为每个考虑的峰包括或排除单键卫星峰方面保持一致。可选使用13C解耦可去除卫星峰并防止它们与其他峰重叠,从而干扰准确定量。13C和31P实验必须使用反向门控去耦,从而防止通过NOE增强信号。
5-2 匀场
将样品插入磁力架后,至少等待5分钟,让样品温度达到平衡。调谐和填充样品,然后运行初始1D光谱。准确的匀场对于定量NMR至关重要,因此如果波谱显示匀场不良的证据(即分辨率差、峰宽或不对称),则重新进行匀场。建议关闭旋转,以防止出现称为“旋转边带”的伪影。如果多次尝试后仍观察到匀场不良,请从磁力架上取出样品,并检查样品量是否可接受,样品是否正确混合,以及核磁管是否干净。
5-3 弛豫延迟
确保所有信号在脉冲之间完全弛豫是至关重要的。使用至少是频谱中目标最慢弛豫信号的T1的五倍的弛豫延迟时间(“d1”)。这里的一个主要问题是样品中核的弛豫时间通常是未知的,尽管它们可以通过反转恢复实验快速估计。中等分子中1H原子核的T1值通常在0.5到4秒之间,而季碳中13C的T1值通常在0.1到数十秒之间。对于非常长的13C弛豫时间,可能需要添加松弛剂。
例如,对于定量质子实验,如果样品中最长的1H T1为4秒,则循环时间应设置为至少20秒。然而,在实践中,循环时间是弛豫时间和采集时间之和。因此,如果采集时间为5秒,则可以将弛豫延迟设置为15秒,总共20秒。如果弛豫时间未知,建议使用以下d1值:1H:30s、19F:30s、31P:30s、13C:60s。
5-4 激发角度
采用90°角激发。与常规氢谱采集时一般采用30°角激发相比,90°角激发可以获得其两倍的信噪比(要获同样的信噪比,若用30°角激发的话,扫描次数要翻4倍)。完全弛豫一般要求D1等待时间是特征峰和内标物峰质子中较长弛豫时间的7倍,而30°角激发,D1等待时间仅能缩短到6倍的特征峰和内标物峰质子中较长弛豫时间。因此,90°角激发是更好的选择。
5-5 频谱窗口
频谱的两侧应有足够的“空白”空间,以确保所需信号不受接收机滤波器引起的衰减的影响。较大的光谱宽度也有助于基线校正。根据经验,应设置光谱宽度,使光谱的末端在每侧延伸约10%的“空白”空间。
5-6 数字分辨率
为了准确积分,每个峰应至少由覆盖线宽的四个数据点来描述,最好是更多。数字分辨率(数据点之间的间距)由光谱宽度(“SW”)除以采集点数(“TD”)的一半定义,这也等于采集时间的倒数(1/AQ)。对于中小分子的典型线宽为1 Hz,因此最小数字分辨率应为0.2 Hz,对应于5秒的采集时间。频谱中的数字分辨率可以使用命令“fidres”来确定。在先前定义了适当的光谱宽度后,应使用参数“td”将数字分辨率设置为至少sw/(td/2)Hz。
5-7 信噪比
良好的信噪比对于精确集成至关重要。对于<1%的集成误差,需要至少250:1的S/N。因此,应设置扫描次数以确保良好的S/N。这将取决于样品的浓度。为了计算频谱中的信噪比,请在topspin中使用“sino”命令。
5-8 激发带宽
共振的均匀激发也是qNMR的基本要求。对于1H光谱,使用标准参数很容易实现这一点,但对于表现出更大化学位移分散的原子核,需要谨慎。由于19F NMR的频率高且化学位移范围较大,这对13F NMR来说是一个特殊问题,但对于13C NMR来说也可能是一个问题。在这种情况下,建议比较具有相似化学位移的共振(并选择能够实现此目的的校准剂),并将频谱中心(定义发射机激发频率“O1P”)置于要比较的峰的中点。采用频率扫描绝热脉冲激发的替代序列可能会提供更好的结果。
6.数据处理
6-1 零填充
确保使用零填充,因为这将提高积分精度。为了使用零填充,必须将实际频谱的大小(“SI”)设置为所用数据点数(“TD”)的倍数。设置SI=TD是零填充的最小量,通常就足够了。
6-2 谱线展宽
建议使用谱线展宽,特别是当频谱具有低S/N时。通常使用指数加权函数。这由参数“LB”控制,默认情况下,1H和1F设置为19 Hz,13C设置为1 Hz。增加线展宽将增加S/N,但会降低分辨率。相反,减小谱线展宽将以牺牲S/N为代价提高分辨率。0.2到1 Hz之间的值是1H和19F光谱的典型值。13C光谱使用更高的值,通常在1-5 Hz范围内。因此,如果需要提高分辨率或S/N,可以通过更改谱线展宽来实现。
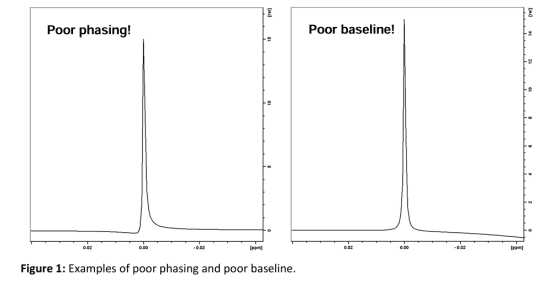
6-3 相位调整
光谱会自动定相(例如。Bruker的“apk”命令)。但是,应检查相位以确保它是最佳的(参见图1)。否则,应手动进行相位调整。
6-4 基线校正
平坦的基线对于准确积分很重要。谱图完成后,基线会自动校正(布鲁克“abs n”命令)。但是,应手动检查基线,并在必要时进行更正(见图1)。
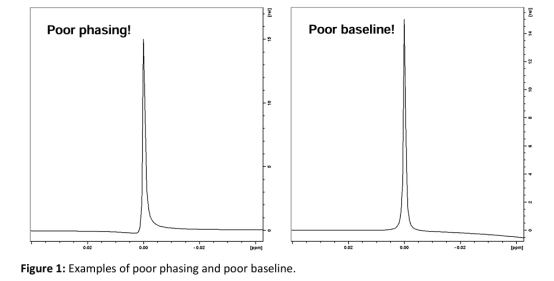
(图1)
6-5 定义适当的积分区域
为了覆盖99%的峰面积,积分区域在每个方向上应覆盖至少20倍线宽(图2)。如果信号重叠是一个问题,可以降低积分限值,但对所有峰使用相同的积分限值很重要。例如,如果每侧的峰积分测量为+/-50 Hz,则所有其他峰也必须测量的+/-50 Hz。此外,如果13C卫星或旋转边带包含在一个峰的积分区中,则所有其他测量的峰都应包括13C卫星或旋转边带。如果信号重叠太严重而不允许适当的积分区域,则可以使用峰值去卷积(例如在mestreNova中)。
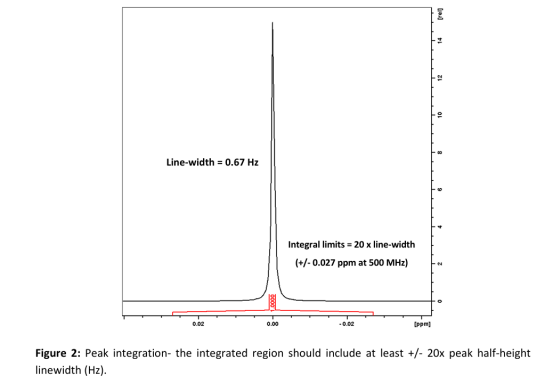
(图2)
溶解性
所选内标物应在所选的代溶剂溶解性好,至少要保证所称量的内标物在所用体积内的氘代溶剂中完全溶解,如果内标物没有完全溶解,则会造成目标化合物含量高于真实值。
7.分析
7-1 定量核磁共振相对浓度测定
基本上,您需要整合感兴趣的信号,对质子数量进行归一化,并进行简单的比率分析。两种化合物x和y之间的摩尔比Mx/My可以使用以下公式确定:
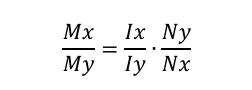
其中I是积分,N是产生信号的原子核数。
7-2 绝对浓度测定
该分析可以得出分析物的浓度,也可以直接提供其纯度的量度。
7-2-1 摩尔浓度
与内标物相对应的信号必须根据产生信号的质子数进行积分和归一化。然后,必须将目标化合物的积分与内标物的积分进行比较。在校准品存在下,化合物x的浓度可使用以下公式计算:
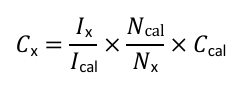
其中I、N和C分别是目标化合物(x)和内标物(cal)的积分面积、原子核数和浓度。这假设内标物的纯度为100%。如果不知道内标物的纯度,则先进行纯度分析可能会有所帮助。
7-2-2 纯度/产量测定
化合物x的纯度(占其标称重量的百分比)可使用以下公式确定:
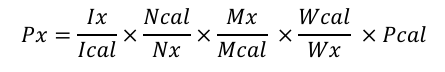
其中,I、N、M、W和P分别是目标化合物(x)和内标物(cal)的积分面积(I)、原子核数(N)、分子量(M)、重量(W)和纯度(P)。因为这是一个基于重量的纯度百分比,所以即使NMR看不到样品中的其他成分,它也能让您评估纯度。
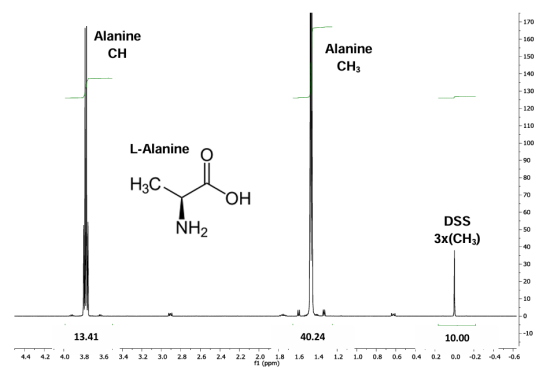
例如,图3说明了氨基酸丙氨酸商业样品的纯度测定。使用1.2 mg DSS(纯度=98%)作为内部校准标准品,测试了1.78 mg丙氨酸的标称质量数。